自2013年6月1日起,新版药品经营质量管理规范(GSP)正式实施,医药企业纷纷采取措施,以应对新一轮的认证与监管要求。对于部分药品经营许可证或药品经营质量管理规范认证证书在2013年12月31日前到期的零售药店,需在2014年6月30日之前完成新版GSP认证。而其他企业则必须在2015年12月31日之前全部完成认证工作,确保符合新标准的规定。
1、 检查系统功能是否完备,管控点是否有效,以及是否与企业介绍的功能模块一致。
2、 检查各岗位操作要点及管控点;确保无遗漏。
3、 检查药品电子监管码时,操作人员需明确具体流程与信息交换方式。
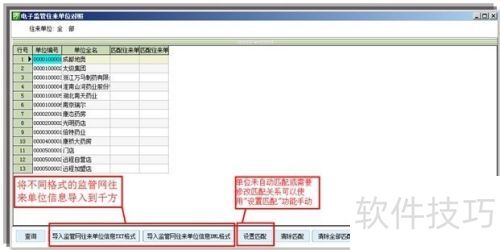
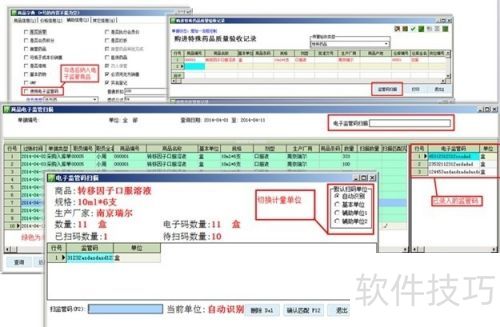
4、 询问岗位人员在遇到质量问题时,于计算机系统中的操作流程。
5、 禁止使用外挂功能,不得以报表替代系统固有功能。
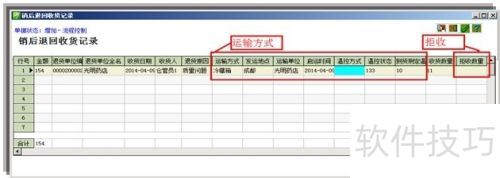
6、 收货员界面需显示物流承运信息,包括在途时间和承运时间,这些信息从采购订单传递至收货员界面。
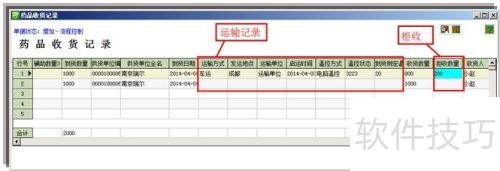
7、 控制冷链品种收货时间,管理温湿度。
8、 药品养护检查需有完整清晰记录,发现质量问题时,应及时处理并记录于计算机系统,同时停止销售与发货。
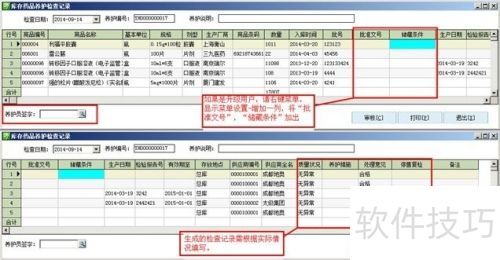
9、 信息部介绍了系统基础数据,涵盖品种分类与管控点范围,包括上下游经营限制、委托书有效期、质保协议及资质时效管理。系统可拦截药品过期情况并提供提示功能。
10、 在采购订单界面中,收货员需核对承运信息,包括承运方式、单位、发运地、在途时间、启动时间和运输方式,并勾兑订单以确认无误。
11、 体系文件的操作流程需与计算机流程一致。
12、 基础数据如品种和供应商信息,由质管部负责录入与更新维护。
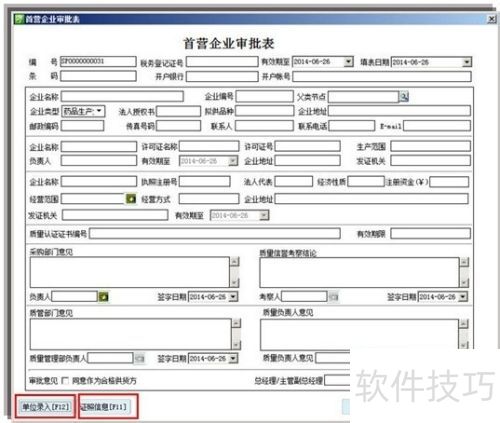
13、 修改经营数据需进行风险评估,并在质管部监督下执行。
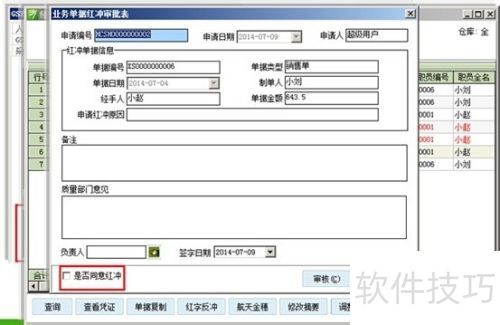
14、 岗位操作权限由质管部授权,人员离职或新增时需重新授权。依据岗位授权配置相应权限,例如收货员不具备分配货位号的权限(此为验收员权限),同时关闭与收货员无关的查询模块。



